식약처, 첨단바이오의약품 장기추적조사 ‘가이드’ 마련
[지디넷코리아]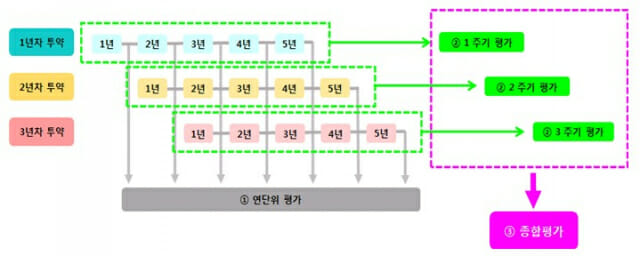
식품의약품안전처가 첨단바이오의약품 장기추적조사를 위한 ‘중대한 이상사례 검토‧처리 지침서’와 ‘장기추적조사 지정 해제 절차’를 마련했다.
첨단바이오의약품 장기추적조사는 줄기세포나 유전물질을 포함하는 첨단바이오의약품을 투여 받은 환자의 안전을 위해 투여 후 장기간에 걸쳐 이상사례 발생 여부를 추적‧조사하는 것이다. 참고로 줄기세포치료제는 5년, 유전자치료제는 15년, 이종이식제제는 30년간 추적 조사가 이뤄진다.
이번에 식약처가 마련한 지침서의 주요 내용은 ▲관련 규정‧가이드라인 ▲적용범위 ▲용어 정의 ▲검토 자료‧절차 흐름도 등 검토지침 ▲접수‧검토‧보완‧결과회신 등이다.

특히 추적‧평가 3년이 종료된 첨단바이오의약품의 장기추적조사 결과를 종합 평가해 장기추적조사 지속 여부를 결정하도록 하는 ‘장기추적조사 지정 해제 절차’도 이번에 함께 마련됐다. 주요 내용은 ▲지정해제 검토대상 ▲평가자료 ▲종합평가‧지정해제 절차 등이다.
식약처는 안정적 운영을 위해 “첨단바이오의약품 장기추적조사 관리기준에도 해당 절차를 반영할 계획”이라고 밝혔다.
한편, 앞서 식약처는 전산망 구축 및 작년 9월 첨단바이오의약품 장기추적조사 실시 절차 안내서도 발간한 바 있다.

